临床试验运行管理制度
Ⅰ、目的
建立本机构药物临床试验运行管理制度,以规范我院药物临床试验过程,保护受试者的权益并保障其安全。
Ⅱ、范围
适用于本机构进行的所有的药物临床试验。
Ⅲ、依据
ü 《药物临床试验质量管理规范》(GCP)
ü 《药品注册管理办法》
ü 《中华人民共和国药品管理法》
ü 《中华人民共和国药品管理法实施条例》
ü 《中华人民共和国疫苗管理法》
ü 《药品不良反应报告和监测管理办法》
ü 《药品生产质量管理规范》(GMP)
Ⅳ、规程
为保证我院药物临床试验过程规范,数据和结果的科学、真实、可靠,保护受试者权益和安全,根据国家药品监督管理局(以下简称NMPA)《药物临床试验机构管理规定管理规定》的通知精神,参照《药物临床试验质量管理规范》(以下简称GCP)等相关法规及文件,结合我院实际情况,制定本管理制度。凡在我院进行的为申请药品注册而进行的药物临床试验,均须按本制度执行。
1.凡在我院进行的药物临床试验由本院药物临床试验机构(以下简称本机构)负责组织实施,由机构办公室具体承办,实行“准入制”,审批权在本机构,未经本机构同意进行的临床试验,概不予认可。
2.凡在我院进行的临床试验必须有充分的科学依据,选择受试者的方法符合科学和伦理要求。周密考虑该试验的目的及要解决的问题,试验方案应当清晰、详细、可操作等等,受试者的权益与安全和是考虑的首要因素,优先于对科学和社会的获益。
3.进行临床试验专业用于临床试验的设施与条件必须满足安全有效地进行试验的需要。主要研究者必须具有本机构的执业资格,具备临床试验所需的专业知识、培训经历和能力,需经过药物临床试验技术要求和相关法规的培训,并获得GCP培训证书。
4.申办者邀请我院参加某项药物临床试验,必须先与机构办公室联系,机构办公室秘书负责对研究者、申办者提供咨询及解释,提供及指导申办方及研究者,填写临床试验立项申请审批表(附件2)同时按临床研究机构初步审查提供文件清单(附件3),要求提供该项目的相关文件。
申办者应提供(不限于):
1) NMPA批准的药物临床研究批件或者公示/其他批准文件;
2) 试验用药品的检验报告;
3) 临床试验方案(注明版本号和日期);
4) 病例报告表(注明版本号和日期);
5) 研究者手册;包括试验药物的临床前研究资料,如处方组成、制造工艺和质量检验结果等。所提供的药学、临床前资料必须符合进行相应各期临床试验的要求;该试验药物已经完成和其它地区正在进行与临床试验有关的有效性和安全性资料;
6) 临床试验药物的制备,应当符合《药品生产质量管理规范》(以下简称GMP)。
以上资料如不完善,我院将拒绝接受。
5.递交资料机构办公室秘书按递交类别进行项目编号,填写“临床试验资料递交函及回执单(附件4)”备案。
1)项目编号:递交资料的临床试验项目由药物临床试验机构办公室统一编号,抄送专业科室,便于项目的管理,项目编号原则:“年份-专业科室-类别(化学药品、生物制品、中成药或诊断试剂、医疗器械)-项目编号”,如2020年,小儿呼吸科专业启动的第一个化学药品项目编号为:“2020-PRD-01-001”。
2)附:化学药品-01;生物制品-02;中成药-03;诊断试剂或医疗器械-04。
6.本机构办公室在接到临床试验申请的15个工作日内,组织相关专业负责人及成员参加审核,必要时组织专家库成员参加审批,根据申办者提供的资料以及专业科室目前进行临床试验的现状,共同讨论是否同意负责或参加该项药物临床试验。
以下情况需专家库成员参加审批:
ü 机构办公室初审认为难度较大、风险性大的项目,在机构决定承接前由机构办公室组织专家库成员进行预审核,确认我院有承接能力,方可进行该试验。
ü 如发生复杂不良事件或者严重不良事件,本专业研究者不能处理,由机构办公室协调专家库专家进行审批。
ü 我院牵头的项目,如果试验中期遇到方案执行困难或者严重影响试验进行的问题,由机构办公室组织专家库成员再次对方案进行审核讨论,与申办方共同讨论方案修改。
7.初步形式和内容审核后,如该试验资料及人员已齐备,机构办公室同意受理,则同意递交伦理委员会审批,并发出 “临床试验受理函及回执单 (CTI-C-005-A01-V2.1)”,研究者及申办者持“临床试验受理函及回执单”共同负责向药物临床试验伦理委员会递交申请,并按照本院伦理委员会的要求提供所需资料,伦理委员会秘书受理申请材料,填写“临床试验受理函及回执单”,由研究者或申办者返给机构办公室备案。
8.项目获得医院伦理委员会批准后,机构办公室根据研究者与申办者达成的有关协议、试验方案与申办者或合同研究组织(以下简称CRO)签订临床试验合同,并送交机构主任审核、签字。我院机构主任批准后方可开始该项试验,相关文件由机构办公室存档。
9.协议签署后,机构办公室向专业科室及其他相关科室下达“临床试验启动通知(附件5)”,报医院业务主管部门批准,报财务主管部门、下发“临床试验检查项目免费通知单”(附件6)。临床试验各项相关申请单,一律由机构办公室统一管理,加盖相应的临床试验印章后方可使用。
10.组织召开机构内部该项目的启动会议,要求该项试验全部研究者及各有关科室的人员参加,由申办者或CRO进行试验前的培训,并共同讨论、制订该项目的工作计划和安排。并按要求保存该药物临床试验各种相关的资料文件。
11.启动会议后,研究者根据试验方案和试验计划、安排,对试验参加人员进行培训:
1) 学习临床研究方案;
2) 学习CRF表填写;
3) 熟悉相关的SOP;
4) 统一试验记录方式与判断标准。
确保试验相关人员履行各自职责,严格遵循试验方案和各项SOP,以保证临床试验的质量控制和质量保证系统的实施。
12.项目负责人审查出现不良事件(以下简称AE)及严重不良事件(以下简称SAE)的预防抢救措施,确保试验场所各项措施切实可行,仪器、设备符合要求。
13.临床试验前需取得受试者的书面知情同意书:
1) 研究者或其指定的研究人员必须向受试者或者其监护人说明有关临床试验的详细情况,并经充分和详细解释试验的情况后获得知情同意书。
2) 如受试者或者其监护人缺乏阅读能力时,则在整个知情过程中应有一名公正的见证人在场,经研究者详细解释知情同意书的内容后,如果受试者或其监护人口头同意,在有能力情况下应当尽量签署知情同意书,见证人还应当在知情同意书上签字和注明日期。
14.试验用药品由申办者提供,严禁向受试者收取费用。使用过程中需建立临床试验用药品接收、保存、发放及回收等记录;
15.临床试验中,根据协议及临床试验方案受试者需要做的相关检查、检验一律免费,不得收费。
16.要求申办者提供其项目负责人、该临床试验主要研究者、监查员的电话、传真、E-mail及其他联系方式,同时向申办者、监查员、该临床试验主要研究者提供本机构主要研究者的电话、传真、E-mail等联系方式,便于互相联系。
17.临床试验开始后,研究人员职责:
1) 必须严格按照试验方案和GCP的要求进行药物临床试验;
2) 认真执行临床试验的SOP;
3) 保证整个临床试验过程均应在严格的随机状态下进行;
4) 应将数据真实、准确、完整、及时地录入临床试验相关病历和CRF;
5) 在试验中必须做到四个一致(检验结果、病历、病例报告表、总结报告);
6) 按GCP规定接受相关监查员的监查;
7) 按计划完成临床试验。
18.在临床试验过程中如发生严重不良事件,研究者的职责:
1) 有义务采取必要的、立即的措施,以保障受试者的安全,并记录在案;
2) 及时报告申办者;涉及死亡事件的报告,研究者应当向申办者和伦理委员会提供其他所需要的资料,如尸检报告和最终医学报告;
3) 如果判断为可疑且非预期严重不良反应,应当报告伦理委员会、申办者;
4) 在严重不良事件报告表上签名及注明日期,随后应当及时提供详尽、书面的随访报告。
19.病历作为临床试验的原始文件,应完整保存。CRF表中的数据来自原始文件,并与原始文件一致,试验中的任何观察、检查结果均应及时、准确、完整、规范、真实地记录于病历和正确地填写至CRF中,不得随意更改。确因填写错误,更正时应保持原记录清晰可辩,保留修改轨迹,必要时解释理由,修改者签署姓名和日期。
20.对临床试验中所有观察的结果和发现都要加以核实,以保证数据的可靠性,确保临床试验中各项结论来源于原始数据。
21.试验项目运行期间,专业项目组需接受申办者委派的监查员的监查,机构办公室质量保证人员(Quality Assurance,以下简称QA)负责对临床试验进度、质量进行检查和监督。
22.临床试验期间,机构办公室的职责:
1) 定期与研究者联系,协调处理试验中出现的问题;
2) 配合药物监督管理部门、申办者委托的稽查、监查人员,完成对临床试验相关活动和文件进行的系统性监查、稽查和检查;
3) 检查试验是否按照既定的试验方案、SOP、进度以及相关法规的要求进行。
23.临床试验完成后,研究者必须及时整理相关记录、表格等资料,撰写总结报告,签名并注明日期后送交机构办公室。项目主要研究者对本项目负责。
24.机构办公室和主要研究者负责对试验资料、数据的科学性、真实性和完整性进行核查;若有问题则要求研究者解答及补充,确认无误后方可将CRF交统计单位。
25.总结报告或分中心小结表需经主要研究者及机构负责人审核、签名/签章,加盖本机构公章,由机构办公室送交申办者。
26.机构办公室出具“临床试验结束通知”附件8。
27.机构办公室按照文件管理程序将该试验过程中的相关文件、资料归档,用于申请药品注册的临床试验,必备文件应当至少保存至试验药物被批准上市后5年,未用于申请药品注册的临床试验,必备文件应当至少保存至临床试验终止后5年。
28.申办者按协议规定支付本机构试验费用,由机构办公室按照“药物临床试验财务管理制度”进行临床试验费用的分配,由财务管理部门分发。
29.为保护申办者的权益,所有参加试验的人员必须严格遵守有关保密法规,对有关该临床试验的所有信息和数据、资料等进行保密。
30.本机构接受药物监督管理部门、申办者委托的稽查人员对临床试验相关活动和文件进行系统性检查,参加临床试验的专业科室和实验室的有关资料及文件(包括病历)接受药物监督管理部门的检查。
Ⅴ、附件
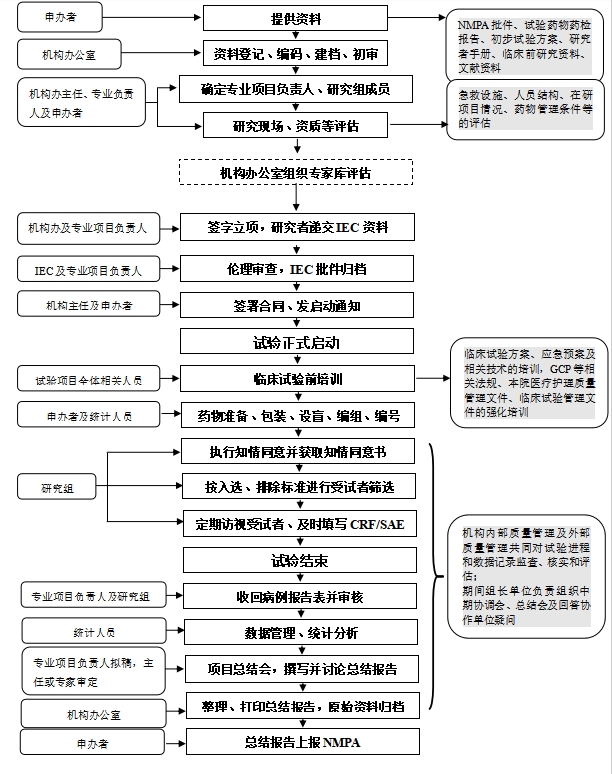
附件1:临床试验运行管理流程图(CTI-A-001-A01-V2.1)
附件2:临床试验立项申请审批表(CTI-A-001-A02-V2.1)
附件3:临床研究机构初步审查提供文件清单(CTI-A-001-A03-V2.1)
附件4:临床试验资料递交函及回执单(CTI-A-001-A04-V2.1)
附件5:临床试验启动通知(CTI-A-001-A05-V2.1)
附件6:临床试验检查项目免费通知单(CTI-A-001-A06-V2.1)
附件7:临床试验结束通知(CTI-A-001-A07-V2.1)
附件1:临床试验运行管理流程图(CTI-A-001-A01-V2.1)
附件2:临床试验立项申请审批表(CTI-A-001-A02-V2.1)
临床试验立项申请审批表
|
申请日期: |
药物临床试验机构受理编号: |
||||||||||
|
申请状态: □初审 □修改后复审 |
|||||||||||
|
该研究方案是否被其他机构拒绝或否决过? □是 □否 |
|||||||||||
|
该研究方案是否曾被暂停或者终止过? □是 □否 |
|||||||||||
|
项目名称 |
|
||||||||||
|
试验类型 |
□Ⅱ期 □Ⅲ期,□Ⅳ期 □器械, □其他 |
||||||||||
|
中国境内同类产品 有□ 无□ |
科室是否使用过同类药物或医疗器械 是□ 否□ |
||||||||||
|
试验用产品 |
□药物 名称 NMPA批件号: |
||||||||||
|
□食品 名称 NMPA批件号: |
|||||||||||
|
□医疗器械 1.□境内II类 □境内III类 □进口II类 □进口III类 2.□有源 □无源 3.□植入 □非植入 |
|||||||||||
|
承担科室 |
|
主要研究者 |
|
||||||||
|
科室联系人 |
|
联系电话 |
|
||||||||
|
申办者/CRO |
|
||||||||||
|
申办联系人 |
|
联系电话 |
|
||||||||
|
申办者地址 |
|
||||||||||
|
中心招募受试者 人数/总人数 |
|
||||||||||
|
预期试验期限 |
|
||||||||||
|
使用方式 |
□创伤性 □非创伤性 |
||||||||||
|
多中心试验 |
□是 □否 |
||||||||||
|
研究形式 |
□Ⅱ期临床试验 □Ⅲ期临床试验 □Ⅳ期临床试验 □生物等效性 □进口药品注册临床试验 □上市药再评价 □临床验证 □流行病学观察 |
||||||||||
|
研究对象 |
□弱势群体 □普通受试者 |
||||||||||
|
受试者年龄范围 |
□<1岁 £1~3岁 □4~14岁 □14~17岁 £自定义年龄范围 |
||||||||||
|
要求排除对象 |
□隔离区 □手术 □静脉输注 □手术 □基因治疗 □义肢 □特殊管理药物(麻醉药、精神药)□妇科 □其他(请具体说明)
□器官移植(请具体说明)
|
||||||||||
|
申办者签字 (盖章) |
|
日期 |
|
||||||||
|
以下由专业科室及机构办填写 |
|||||||||||
|
专业科室评估: 1. 是否能保证招募足够的受试人群: 是□,否£ 2. 专业的病种开展情况能够满足试验的需要: 是□,否□ 3. 研究者是否具备足够的试验时间: 是□,否□ 4. 是否具备相应的仪器设备和其他技术条件:是□,否□ 5. 目前科室承担的与试验药物疾病相同的在研项目:无□,1项□,2项□,2项以上□ 6.专业正在开展的临床试验项目: 项,具体如下:
7.主要研究者: 评估意见:同意□,不同意□ 主要评估者签字: 日期: 年 月 日 |
|||||||||||
|
机构办公室评估: 1. 临床前研究资料是否齐全:是□,否□ 2. 临床科室承担项目的能力:强□,一般□,弱□ 3. 申办者对试验过程质量保证的能力:强□,一般□,弱□ 评估意见:同意□ → 项目联络员: 主要研究者: 不同意□
机构办公室主任签字(盖章): 日期: 年 月 日 |
|||||||||||
|
伦理办公室意见: (如不同意请注明原因) 附:批件或伦理受理意见通知函 伦理受理号:________________ □同意 □作必要的修正后同意 □作必要的修正后重审 □不同意
|
|||||||||||
附件3:临床研究机构初步审查提供文件清单(CTI-A-001-A03-V2.1)
II/Ⅲ/Ⅳ期临床研究机构初步审查提供文件清单(不限于)
|
1. |
临床试验申请审批表(申请者签名、盖章并签署日期) |
|
2. |
国家药品监督管理局药物临床试验批件或准许文件/公示 |
|
3. |
申办者资质证明及委托函 |
|
4. |
试验用药品检验合格报告 |
|
5. |
临床试验方案摘要 |
|
6. |
临床试验方案(注明版本号和日期) |
|
7. |
病例报告表(注明版本号和日期) |
|
8. |
知情同意书(注明版本号和日期) |
|
9. |
研究者手册(注明版本号和日期) |
|
10. |
多中心研究单位一览表(如有) |
|
11. |
研究者履历及相关文件 |
|
12. |
所有以前其他机构、伦理委员会或管理部门对申请研究项目的重要决定的说明,应提供以前否定结论的理由 |
|
13. |
其他资料(如受试者须知、受试者日记、紧急联系卡、招募广告、保险声明等) |
附件4:临床试验资料递交函及回执单(CTI-A-001-A04-V2.1)
临床试验资料递交函及回执单
|
项目名称 |
|
|||
|
研究类别 |
|
|||
|
申办者 |
|
递交日期 |
|
|
|
联系人 |
|
联系方式 |
|
|
|
承担科室 |
|
主要研究者 |
|
|
|
科室联系人 |
|
联系方式 |
|
|
|
徐州市儿童医院 药物临床试验机构办公室: 按机构办公室要求,本研究现提供以下资料,请机构办公室审阅, |
||||
|
□临床试验立项申请审批表(申请者签名、盖章并签署日期); □国家药品监督管理局药物临床试验批件或批准公示 □申办者资质证明及委托函; □试验用药品检验合格报告; □临床试验方案摘要; □临床试验方案(注明版本号和日期); □病例报告表(注明版本号和日期); □知情同意书(注明版本号和日期); □研究者手册(注明版本号和日期); □多中心研究单位一览表(如有); □研究者履历; □所有以前其他机构、伦理委员会或管理部门对申请研究项目的重要决定的说明,应提供以前否定结论的理由; □其他资料(如受试者须知、受试者日记、紧急联系卡、招募广告、保险声明等)。 |
||||
|
递交人(签字): |
|
日期: |
|
|
… … … … … … … … … … … … … … … … … … …
资料递交回执单
|
项目名称 |
|
|
项目编号 |
|
|
: 药物临床试验机构办公室已收到上述研究项目的递交函。 机构办公室受理人签字: 日期 (盖章) |
|
附件5:临床试验启动通知(CTI-A-001-A05-V2.1)
临床试验启动通知
各相关部门,我院现已承接由 公司申请的 临床试验,预计开始时间 请各部门做好相应准备,特此通知。
药物临床试验机构办公室
年 月 日
|
项目名称 |
|
||||
|
试验类型 |
Ⅱ期□,Ⅲ期□,Ⅳ期□,生物等效性试验□,器械□,其他□ |
||||
|
预计承担例数 |
|
承担科室 |
|
||
|
机构项目 联络人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
专业科室 联系人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
申办者或者 CRO单位名称 |
|
||||
|
申办方联系人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
抄送:申办方、 科、检验科、心电图室、伦理委员会、财务科 |
|||||
附件6:临床试验检查项目免费通知单(CTI-A-001-A06-V2.1)
临床试验检查项目免费通知单
|
项目名称 |
|
||||
|
试验程序 |
单价 |
检查次数 |
例数 |
单项共计 |
|
|
实验室常规检查
|
血常规 |
|
|
|
|
|
尿常规 |
|
|
|
|
|
|
便常规 |
|
|
|
|
|
|
|
|
|
|
|
|
|
血生化 |
生化 项 |
|
|
|
|
|
12-导联心电图 |
|
|
|
|
|
|
心脏超声 |
|
|
|
|
|
|
胸片 |
|
|
|
|
|
|
CT |
|
|
|
|
|
|
MRI |
|
|
|
|
|
|
其他 |
|
|
|
|
|
|
........ |
|
|
|
|
|
|
费用共计 |
|
||||
附件7:临床试验结束通知(CTI-A-001-A07-V2.1)
临床试验结束通知
各相关部门,我院所承担的 公司申请的 临床试验,现已全部完成,完成日期: 。特此通告。
药物临床试验机构办公室
年 月 日
|
项目名称 |
|
||||
|
试验类型 |
Ⅱ期□,Ⅲ期□,Ⅳ期□,生物等效性试验□,器械□,其他□ |
||||
|
实际承担例数 |
|
承担科室 |
|
||
|
机构项目 联络人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
专业科室 联系人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
申办者或者 CRO单位名称 |
|
||||
|
申办联系人 |
|
联系电话 |
|
||
|
|
|
||||
|
手机 |
|
||||
|
抄送:申办方、 科、检验科、伦理委员会、财务科 |
|||||

